口服劑型仍然是患者可用的zui靈活和有效的治療方法之一。溶出度測試是所有固體口服劑型的要求,并且在整個開發生命周期中用于產品釋放和穩定性測試。它是用于檢測活性藥物成分和配制產品的物理變化的關鍵分析測試。在藥物開發過程的早期階段,體外溶出度測試支持從給定制劑中優化藥物釋放。
口服劑型的有效性取決于藥物在被吸收到循環中之前溶解在胃腸道液體中的內在能力。因此,片劑或膠囊的溶出速率對該過程是關鍵的。
藥物開發中遇到的關鍵問題之一是需要優化身體可用的藥物水平以獲得其所需的治療效果。在治療窗外的這種不正確的優化可能潛在地導致生物利用度不足(因此缺乏功效)或相反地,生物利用度太高,從而對患者產生不希望的不良毒性作用。
為了有助于劑型優化,溶出度測試是用于測量給定劑型的藥物釋放速率的標準化方法。
盡管是制藥和生物制藥行業中常用的測試,但溶出測試的基本原理往往得不到正確理解。該測試必須具有穩健性和可重復性,能夠檢測產品性能的任何關鍵變化,即區分不同的配方和/或批次。
所用的確切溶出技術由劑型特征和預期的給藥途徑決定。對于固體劑型,工業標準溶出測試方法是美G藥典(USP)裝置I(籃子)和USP裝置2(槳葉)。立即,改良和延長釋放通常在具有USP 2槳的標準溶解浴中進行測試。對于易于漂浮的口服劑型,通常需要USP 1(籃子)。除了上述設備類型之外,還有其他技術可用,例如USP 3(往復式汽缸),USP 4(流通式電池),USP 5(槳式換盤),USP 6(汽缸)和USP 7。 (往復式支架)。
在開發溶出儀過程方面,需要評估幾個方面以實現穩健的方法。必須評估設備類型,介質和攪拌速率等因素,并且這些因素應適合于所測試的產品。出于本文的目的,將討論zui常見的技術(USP設備1和2),包括在開發溶出方法時應考慮的典型方法參數的概述。
為了使劑型有效,必須提取API(溶解在溶液中)然后吸收到體循環中以促進其轉運到活性部位。該過程影響API的總體生物利用度。了解這一過程是進行體外方法開發的基礎。溶解是將API從固體劑型提取到溶液中的過程。下面給出了一個簡單的圖示:
圖1:一個固體口服劑型的溶出
一旦API處于溶液中,就可以發生吸收過程,由此藥物物質從胃腸腔進入循環系統,然后它可以進入相關的受體部位以發揮生物反應。
溶出度是一種體外測試,用于評估API如何從固體劑型中提取。它可以提供體內溶出效率的指示,但jue不提供任何藥物吸收的數據。為了評估后者,需要產生藥代動力學數據并用于補充溶出工作。
如果選擇合適的體外條件并進行適當評估(以模擬體內條件),它可以幫助確定成功的體外 - 體內相關性(IVIVC),或者zui壞的情況下,確定兩者之間的關系。應該注意的是,對于QC目的而言zui佳的溶出參數可能不適合建立IVIVC,因此可能需要兩次溶出試驗以滿足開發和監管需求。
在開發溶出方法時,重要的是對該過程采取合理的系統方法,并確保牢記科學和監管原則。穩健的溶出方法應該沒有明顯的干擾(例如由賦形劑引起的基質效應),產生低的可變性(精確度)并產生良好的輪廓形狀。該方法還應該受到挑戰,以區分具有不同質量屬性的批次材料。一旦確定合適的培養基和裝置的過程完成,就需要進一步優化該方法以評估培養基的離子強度,攪拌速率和(如果需要的話)表面活性劑濃度。zui終開發的方法應該能夠區分不同的配方/批次,但仍保持可接受的精度和穩健性。關于精確度,早期和晚期時間點的典型限制將分別<20%和<10%RSD。

圖2:典型的溶解浴裝置
水槽條件
沉降條件定義為“溶液濃度通常對應于溶解介質中API的標稱工作濃度的5-10倍”。確定水槽的實現對于建立合適的溶解方法至關重要。如果不能實現這些(并且因此介質達到飽和點),則不能始終如一地測量溶解速率。重要的是,在進行溶出試驗時,對結果的**影響應該是產品的攪拌速率和溶解度。
媒體
篩選潛在培養基時的zui初焦點是從水基的那些開始,在推薦的離子強度的1.2-6.8的pH范圍內(根據USP / EP)。當評估在整個pH范圍內在水性介質中顯示低溶解度的API時,建議加入表面活性劑,盡管使用的水平應盡可能低。
劑型
在方法開發階段,應考慮劑型類型(膠囊,片劑等),強度,賦形劑,釋放類型(即時,持續,延遲),穩定性數據和表面涂層的基本特征。此外,制造變量對于評估不同配方之間API釋放的差異也是關鍵。完善的溶出方法應該允許區分各種產品屬性。
進行溶解時,將在設定的時間點取出樣品,并繪制相對于時間的溶解百分比(如下圖3所示):
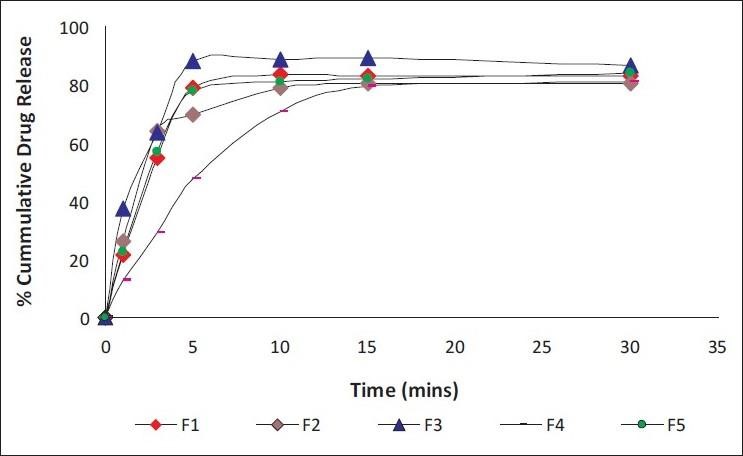
圖3:不同制劑之間溶出曲線表示歧視
在溶出度分析的整個過程中,確保維持目視觀察至關重要。這可以提供額外的數據來支持分析結果中的任何數量差異。
需要建立溶解的分析結果。在可能的情況下,為了保持簡單性和效率(并假設存在合適的發色團),可以采用簡單的UV涂飾; 這也需要獲得合適的特異性以確保活性物質的吸光度不受任何其他干擾的影響。
通常,使用HPLC-UV進行定量。這通常是有利的,以便減少/消除可能以其他方式損害獨立UV方法的干擾。另外,通過縮短運行時間以允許溶出分析所需的高樣品通量,很可能先前的HPLC測定方法適用于溶出樣品。HPLC還提供了調節進樣體積的靈活性,以適應不同產品強度可能需要的樣品濃度變化。
在某些情況下,它可能是篩選材料的元素組分的實際替代品,例如對于活性材料是無機鹽的產品,或者在傳統檢測有問題的情況下,則可以監測計數器取而代之的是鈉或鈣等離子。
有許多元素光譜技術可用于此目的。儀器的選擇取決于所需的分析物和溶液中的預期濃度。
例如,溴化鉀片劑的溶出曲線可以通過使用火焰原子吸收光譜法(FAAS)來測量鉀的水平,或者溴化物的濃度(以元素溴測量)可以通過電感耦合等離子體質量來測量。光譜法(ICP-MS)。另一個應用可能是使用電感耦合等離子體 - 光學發射光譜(ICP-OES)來確定從富馬酸亞鐵片溶出的溶液中鐵的含量
總之,合適的溶出程序的設計必須考慮到API,配方和分析方法的許多參數。體外溶出度測試應提供強大的數據體,以確保產品性能和質量。在整個過程中,重要的是確保體外溶出類似于體內條件。如果有效地設計溶出程序,它將加速藥物開發,并且理想地減少對人類研究的需要。